신개발의료기기의 시장진입이 신속히 이뤄질 것으로 보인다.
식품의약품안전처(처장 이의경)와 한국보건의료연구원(원장 한광협)은 27일 “식약처의 허가도우미와 보의연의 신의료기술평가를 시범 연계 운영한다”고 발표했다.
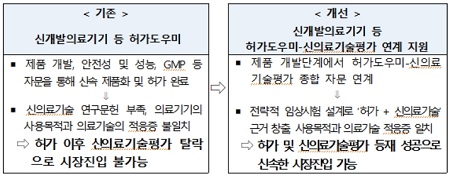
지원사업은 허가도우미로 지정된 △손상된 각막을 대체하기 위한 인공각막 △암치료를 위한 치료용중성자조사장치 △증강현실(AR)을 이용하여 시술할 병변의 위치를 표시하는 기기 등 3개 분야는 27일부터 시행된다. 또 ▲허가단계부터 신의료기술평가를 고려한 임상 설계 ▲개발제품 사용목적 구체화 ▲제조 및 품질관리시스템(GMP) 검토 ▲안전성 및 성능 검토 등 전주기 컨설팅을 실시할 계획이다.
특히, ‘임상시험 설계 자문’을 통해 허가를 위한 임상시험 계획 설계단계에서 신의료기술평가를 동시에 고려할 수 있어, 안전성·유효성 연구결과의 미흡으로 시장진입이 어려워지는 것을 해소할 수 있을 것으로 예상된다.
두 기관은 이번 협력으로 신개발의료기기의 시장진입 기회가 확대될 것으로 전망하고 있다.
이 기사를 공유합니다

